波义耳定律(又称马里奥特定律、波义耳-马里奥特定律)是关于理想气体的定律。
该法可说明如下:
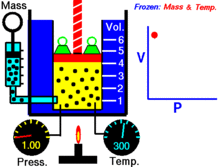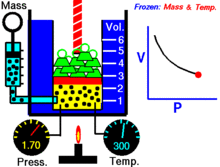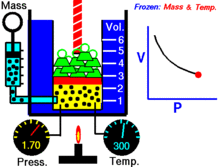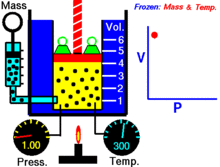
换句话说,恒定质量的理想气体在恒定温度下的体积与施加在它身上的压力成反比。
在符号中,法律是。
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}}.
或
P V = k {\displaystyle PV=k}。
对于给定质量的气体,在恒温下,压强和体积的乘积是一个常数。当体积减小时,压强会按比例增加,反之亦然。例如,当压强减半时,体积增加一倍。
假设你有一个罐子,在一定压力下装有一定体积的气体。当你减小罐子的体积时,同样数量的气体颗粒现在被装在一个较小的空间里。因此,碰撞的次数就会增加。因此,压力更大。
想象一下,你有一个气体在一定的压力(P1)和体积(V1)。如果你把压力改变到一个新的值(P2),体积就会改变到一个新的值(V2)。我们可以用波义耳定律来描述这两组条件。
P 1 V 1 = k {displaystyle P_{1}V_{1}=k}.
P 2 V 2 = k {displaystyle P_{2}V_{2}=k}.
常数k在两种情况下都是一样的,所以我们可以这样说。
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}。
例子:一个气体的压力是3大气压,体积是5升。一种气体的压力是3大气压,体积是5升。如果压力降低到2个大气压,体积是多少?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}。
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}}{P_{2}}}}。
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={/frac {3*5}{2}}}。
V 2 = 15 2 {\displaystyle V_{2}={\frac {15}{2}}}}。
V 2 = 7.5 {displaystyle V_{2}=7.5}。
∴容积为7.5升。
该法由罗伯特-博伊尔于1662年发现,之后由埃德姆-马里奥特于1679年独立发现。