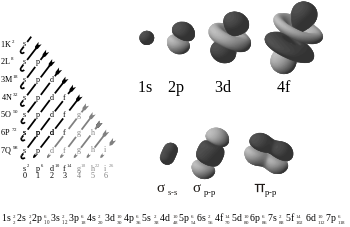
在化学中,∏键(π键)是一种电子的轨道与另一种电子的轨道交叉(重叠)的共价化学键。电子的路径呈叶形八字形(见图)。有两个重叠的区域,因为两个裂片上的路径是重叠的。只有一个轨道的结点平面通过两个相关核。
它们名字中的希腊字母π指的是p轨道。从键轴向下看,pi键的轨道对称性与p轨道看起来是一样的。p轨道通常有这种键。D轨道也被认为使用pi键,但现实中不一定是这样。d轨道成键的想法与超值理论相吻合。
Pi键通常比Sigma键弱。量子力学说,这是因为轨道路径是平行的,所以p轨道之间的重叠要少得多。
当两个原子轨道通过两个重叠区域接触时,就会发生π键。皮键是比西格玛键更分散的键。∏键中的电子有时被称为∏电子。由∏键连接的分子碎片如果不破坏∏键,就不能围绕该键旋转。旋转破坏了两个p轨道的平行路径。