共价键是两个非金属原子之间的化学键。一个例子是水,其中氢(H)和氧(O)结合在一起形成(H2O)。一个完整的外壳通常有八个电子,如果是氢或氦,则有两个电子。价电子是指原子外壳中相对松散地持有的电子。电子壳的结构是由量子力学决定的)。)
原子中电子的数量是由原子中质子的数量决定的。电子绕着原子核运行,它们就像围绕原子核的模糊轨道。第一层最多有两个电子。之后的各层通常最多包含8个电子。共价键是由原子共享价电子形成的。
例如,如果一个原子有9个电子,前两个电子的轨道离原子核很近,后7个电子的轨道离原子核稍远。外侧的7个电子比内侧的2个电子保持得不那么紧,因为它们离带正电的原子核更远。如果这个原子靠近另一个原子,其外层有一个松散保持的电子,一个新的轨道就会成为松散保持的电子的可用轨道。这个新的电子轨道与两个原子核结合在一起,并且比原来的电子轨道的能级低。电子可以自发地跳到它那里,并发射出具有多余能量的光子。现在我们有一个电子在两个原子轨道上运行,这就导致提供电子的原子有一个小的净正电荷,而另一个原子有一个小的净负电荷。现在两个原子通过正电荷和负电荷之间的电磁吸引力结合在一起。这就是所谓的共价键。要打破这个键需要与形成时释放的能量相同的能量。
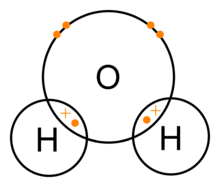
水分子由一个氧原子和两个氢原子通过共价键结合在一起。在这种情况下,氧原子与每个氢原子共享一个电子。这意味着氧原子带有较小的净正电荷,氢原子带有较小的净负电荷。因此,由于电磁力的作用,氧原子和氢原子相互吸引。正因为如此,水分子是一个极性分子:它的电荷分布不均匀。