李子布丁模型是20世纪早期(也是不正确的)的原子模型。它是由J.J.汤姆森在1904年提出的,在发现电子之后,但在发现原子核之前。在那个时候,科学家们知道原子中有一个正电荷,它平衡了电子的负电荷,使原子呈中性,但他们不知道这个正电荷来自哪里。汤姆森的模型显示,原子有一个带正电的介质,或空间,介质内有带负电的电子。在其提出后不久,该模型被称为 "李子布丁 "模型,因为正的介质就像布丁,里面有电子,或李子。
李子布丁模型
发展为现代原子模型
卢瑟福的模型
基本上,在1909年,在汤姆森的模型被提出后不久,汉斯-盖格和欧内斯特-马斯登用薄金片做了一个实验,以测试汤姆森的模型。他们的教授欧内斯特-卢瑟福期望实验结果能证明汤姆森是正确的,但他们的结果与他们所期望的极为不同。1911年,卢瑟福发现,正电荷来自被称为质子的微小粒子,质子在一个被称为原子核的微小中心,而电子则围绕原子核运行。
玻尔模型
卢瑟福的模型相当简单,但它是错误的,因为电子有电荷,它们应该被吸引到带正电的原子核。1913年,尼尔斯-玻尔在原子模型中加入了 "能级"。电子不会落入原子核,因为它们被包含在能级中,要改变到更高的能级需要额外的能量,而要改变到较低的能级则需要释放能量。如果不改变电子的能量,就不可能改变能量状态。如果一个电子被一个光子(一种携带电磁辐射的粒子)击中,它将获得额外的能量并进入一个更高的能级(它改变了状态),然后它将跳回一个较低的能级,释放其包含的能量。这个新模型被称为玻尔模型或卢瑟福-玻尔模型。这增加了一个全新的科学分支。量子物理学。
量子模型
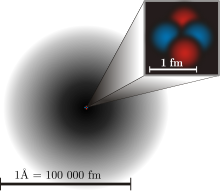
1926年,埃尔温-薛定谔提出了电子既是波,又是粒子的观点,这被称为波粒二象性。这给原子模型和量子物理学增加了一个全新的层次。对于一个粒子,如果你观察(看)它,你可以知道它在空间的位置。但对于波来说,它到处都是,所以你无法定义它的确切位置。这就是所谓的量子不确定性。对于电子,你只能知道它在某个地方的概率,因为它是一个波,也是一个粒子。(见上图)
相关页面
- 原子理论
- 量子力学
- J.J. 汤姆森
- 欧内斯特-卢瑟福
- 尼尔斯-玻尔
- Erwin Schrödinger