早期实验
公元前2世纪,拜占庭的希腊人Philo进行了关于燃烧如何需要空气的第一个已知实验。他在他的著作《Pneumatica》中写道,将一个容器倒置在燃烧的蜡烛上,并在这个容器周围放水,意味着一些水进入了容器。斐洛认为这是因为空气变成了古典元素火。这是错的。很久以后,达芬奇正确地研究出,当燃烧发生时,空气被用掉了,这就迫使水进入容器。
17世纪末,罗伯特-波义耳发现,燃烧需要空气。英国化学家约翰-马约对此进行了补充,证明火只需要一部分空气。我们现在称之为氧气(以二氧的形式)。在他的一个实验中,他发现把蜡烛放在一个封闭的容器中,在熄灭之前,会使水上升,取代容器中空气体积的十四分之一。把一只老鼠放进盒子里,也发生了同样的事情。由此,他研究出氧气是用来呼吸和燃烧的。
闪电理论
罗伯特-胡克、奥勒-波尔奇、米哈伊尔-罗蒙诺索夫和皮埃尔-巴彦都在17、18世纪的实验中制造出了氧气。他们都不认为它是一种化学元素。这可能是因为phlogiston理论的想法。这是大多数人认为引起燃烧和腐蚀的原因。
J.J. Becher在1667年提出了这一理论,Georg Ernst Stahl在1731年对其进行了补充。phlogiston理论指出,所有的可燃物都由两部分组成。一部分称为phlogiston,当含有它的物质燃烧时,它就会被释放出来。
只留下少量残留物的非常易燃的材料,如木材或煤,被认为是由菲林斯顿制成的。腐蚀的东西,如铁,被认为只含有少量的物质。空气不属于这一理论的范畴。
发现
波兰炼金术士、哲学家和医生迈克尔-森迪沃吉乌斯谈到空气中的一种物质,称它为"生命的食物".,这种物质就是氧气。仙迪沃吉乌斯在1598年到1604年之间发现,这种物质与硝酸钾热分解过程中产生的物质是一样的。有人认为这是氧气的发现,也有人不同意。
通常也有人说,氧气是由瑞典药剂师卡尔-威廉-谢勒首先发现的。1771年,他通过加热氧化汞和一些硝酸盐来制造氧气。Scheele称他制造的气体为"火气",因为它是已知唯一可以燃烧的气体。他于1777年发表了他的发现。
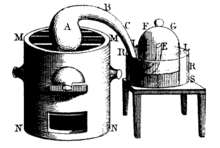
1774年8月1日,英国神职人员约瑟夫-普里斯特利进行了一项实验,将太阳光聚焦在玻璃管中的氧化汞上。这就产生了一种被他称为"除雾空气"的气体。他还发现,蜡烛在这种气体中燃烧得更亮,老鼠在呼吸这种气体时寿命更长。当他呼吸这种气体时,他说(简化版)"感觉就像正常的空气一样,但我的肺在之后感觉更轻盈、更轻松"。他的发现在1775年发表。因为他的发现是最先发表的,所以通常说他是氧气的发现者。
法国化学家Antoine Lavoisier后来说他也发现了这种物质。1774年,普里斯特利去拜访他,告诉他他的实验情况。Scheele也在这一年给Lavoisier写了一封信,信中谈到了他的发现。
拉瓦锡的贡献
拉瓦锡进行了第一个关于氧化的主要实验,并对燃烧的原理作出了第一个正确的解释。他用这些实验和其他实验证明了phlogiston理论的错误。他还试图证明普里斯特利和舍勒发现的物质是一种化学元素。
在一次实验中,拉瓦锡发现,锡和空气在密闭容器中加热时,质量没有增加。他还发现,当容器被打开时,空气涌入。此后,他发现锡的质量增加的量与冲入的空气的质量增加的量相同。他在1777年发表了他的发现。他写道,空气是由两种气体组成的。一种他称为"生命之气"(氧气),它是燃烧和呼吸所需要的。另一种他称为"氮气"(azote),在希腊语中是"无生命"的意思。在包括法语在内的一些语言中,这仍然是氮气的名称。
拉瓦锡将"生命之气"改名为"氧气",希腊语的意思是"酸的生产者"。他之所以这样叫,是因为他认为所有的酸中都有氧,这是错误的。许多化学家意识到拉沃泽的命名是错误的,但当时这个名字已经太普通了,无法更改。
"氧气"成了英语中的名称,尽管英国科学家反对。
后来的历史
约翰-道尔顿的原子理论说,所有元素都有一个原子,化合物中的原子通常是单独存在的。例如,他错误地认为水(H2O)的公式只有HO。1805年,约瑟夫-路易-盖-吕萨克和亚历山大-冯-洪堡证明,水是由两个氢原子和一个氧原子组成的。到了1811年,阿梅迪奥-阿伏加德罗根据阿伏加德罗定律正确地研究出了水的构成。
到了19世纪末,科学家们发现,空气可以变成液体,其中的化合物可以通过压缩和冷却来分离。瑞士化学家和物理学家拉乌尔-皮克泰通过蒸发二氧化硫使二氧化碳变成液体,发现了液态氧。然后也蒸发冷却氧气气体,以使其变成液体。他于1877年12月22日给法国科学院发了一封电报,告诉他们他的发现。