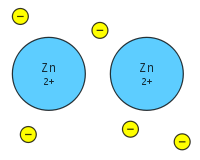
金属键是许多正离子之间共享许多分离的电子,电子作为一种"胶水"使物质具有确定的结构。它不同于共价键或离子键。金属的电离能量很低。因此,价电子可以在整个金属中脱位。错位电子不与金属的某一特定原子核相关联,相反,它们可以在整个晶体结构中自由移动,形成电子的"海洋"。
金属中的电子和正离子之间有很强的吸引力。因此,金属的熔点或沸点往往很高。其原理与离子键的原理相似。
金属键造成金属的许多特性,如强度、可塑性、延展性、光泽、导热和导电。
由于电子自由移动,金属具有一定的导电性。它可以让能量快速通过电子,产生电流。金属导热也是出于同样的原因:自由电子可以比其他电子固定在位置上的物质以更快的速度传递能量。也有少数非金属能导电:石墨(因为和金属一样,它也有自由电子),以及熔融或溶解在水中的离子化合物,它们有自由移动的离子。
金属键至少有一个价电子,它们不与相邻原子共享,也不会失去电子形成离子。相反,金属原子的外层能级(原子轨道)是重叠的。它们类似于共价键。并非所有金属都表现出金属键。例如,汞离子(Hg2+)
2)形成共价金属金属键。
合金是金属的溶液。大多数合金像纯金属一样有光泽。