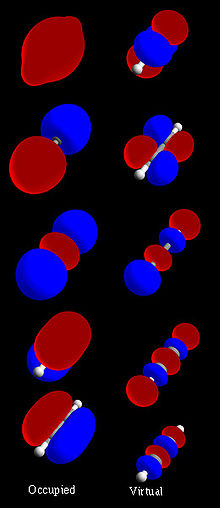
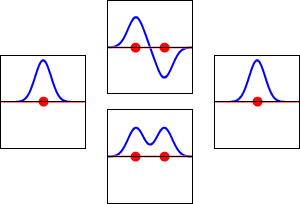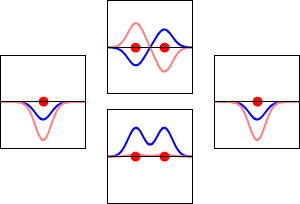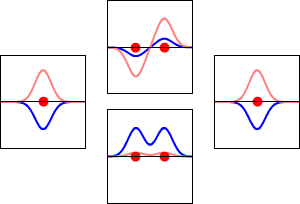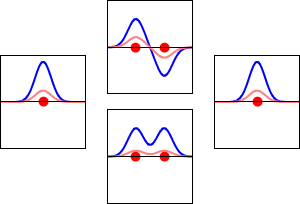
化学家需要了解MOs的几何学,才能讨论分子结构。LCMO(线性组合原子轨道分子轨道)方法对MOs给出了一个粗略但很好的描述。在这种方法中,分子轨道被表示为分子中每个原子的所有原子轨道的线性组合。
原子轨道的线性组合(LCAO)
分子轨道最早由弗里德里希-亨德和罗伯特-S-穆利肯于1927年和1928年提出。
原子轨道的线性组合或分子轨道的"LCAO"近似是由John Lennard-Jones爵士在1929年提出的。他的开创性论文显示了如何从量子原理推导出氟和氧分子的电子结构。这种分子轨道理论的定性方法是现代量子化学的开端之一。
原子轨道的线性组合(LCAO)可以用来猜测分子的原子结合在一起时的分子轨道。与原子轨道类似,描述电子行为的薛定谔方程也可以构建分子轨道。原子轨道的线性组合,(原子波函数的和与差)提供了分子薛定谔方程的近似解。对于简单的二原子分子,你得到的波函数在数学上用方程来表示
Ψ = caψa + cbψb
和
Ψ* = caψa - cbψb
其中Ψ和Ψ*分别是成键和反键分子轨道的分子波函数,ψa和ψb分别是来自原子a和b的原子波函数,ca和cb是可调系数。这些系数可以是正的或负的,取决于各个原子轨道的能量和对称性。当两个原子的距离越来越近时,它们的原子轨道就会重叠,产生高电子密度的区域。所以,两个原子之间就形成了分子轨道。带正电的原子核和占据键合分子轨道的带负电的电子之间的静电吸引将原子固定在一起。
粘结、反粘结和非粘结性MOs
当原子轨道发生相互作用时,产生的分子轨道可以有三种类型:成键、反成键或非成键。
粘合MOs。
- 原子轨道间的键合作用属于建构(相位)作用。
- 键合MOs的能量比结合产生它们的原子轨道要低。
抗粘结性MOs。
- 原子轨道间的反键作用是破坏性(相外)作用。
- 反键MOs的能量高于结合产生它们的原子轨道。
非粘结性MOs。
- 非键合MOs是由于原子轨道之间没有相互作用,因为缺乏相容的对称性。
- 非键合MO将具有与分子中某一原子的原子轨道相同的能量。
HOMO和LUMO
每个分子轨道都有自己的能级。化学家按能级对分子轨道进行排序。化学家假设电子将首先填满能级最低的MOs。例如,如果一个分子有电子可以填满15个轨道,那么15个能级最低的MO将被填满。列表中的第15个MO将被称为"最高占用的分子轨道"(HOMO),列表中的第16个MO将是"最低未占用的分子轨道"(LUMO)。HOMO的能级与LUMO的能级之差称为带隙。带隙有时可以作为衡量分子可激发性的标准:能量越小,越容易被激发。当电子被激发时,它将跳到一个未被占据的MO上。例如,这可以帮助猜测某物是否会发出光(发光)。