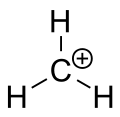
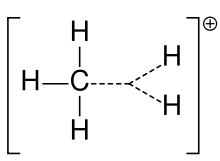
羰基是一种带有正电荷的碳原子的离子。碳配位中带电的碳原子是 "六价"(也就是说,它的外层价层中只有六个电子,而不是八个价层电子)。具有八个价选的碳原子具有最大的稳定性(八重性规则)。因此,碳配位体往往是反应性的,寻求填补八价电子,以及重新获得中性电荷。从逻辑上讲,碳化物有sp3杂化,空的sp3轨道给正电荷。然而,碳化物的反应性更接近于sp2杂化和三棱柱分子的几何形状。
碳正离子
定义
羰基化合物以前常被称为碳离子,但化学家对其确切含义提出质疑。在今天的化学中,碳配位是任何带正电的碳原子。有人提出两种特殊的类型:碳铵离子是三价的,而碳离子是五价或六价的。大学水平的教科书在讨论碳配位时只把它们当作是碳铵离子,或者在讨论碳配位时稍稍提到碳铵离子或碳铵和碳铵离子这一较早的说法。有一本教科书至今仍使用旧的碳离子名称来表示碳酸盐离子,并将超价碳酸盐离子这一短语保留给CH5+。
历史
1891年,G.Merling报告说,他将溴加入到托匹林(环庚三烯)中,然后将产品加热,得到一种结晶性的水溶性物质,C
7H
7他没有提出它的结构;但是Doering和Knox令人信服地表明,它是溴化托匹里尼(环庚三烯)。根据Hückel规则,这种离子被预测为芳香族。
1902年,Norris和Kehrman独立发现,无色的三苯甲醇在浓硫酸中产生深黄色的溶液。三苯甲基氯同样与氯化铝和氯化锡形成橙色的络合物。1902年,Adolf von Baeyer认识到所形成的化合物的盐类特性。
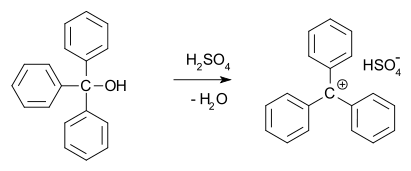
他把颜色和盐的形成之间的关系称为卤素色,孔雀石绿就是一个最好的例子。
碳化物是许多有机反应中的反应性中间物。这个观点是由Julius Stieglitz在1899年首次提出的,由Hans Meerwein在1922年对Wagner-Meerwein重排的研究中进一步发展。人们还发现碳化物参与了NS1反应、E1反应和重排反应,如Whitmore 1,2转移。化学界不愿意接受碳化物的概念,在很长一段时间里,《美国化学会杂志》拒绝了提到碳化物的文章。
Doering等人在1958年发表了溶液中稳定碳化物的第一个核磁共振谱。它是七甲基苯离子,通过用二氯甲烷和氯化铝处理六甲基苯而制成。稳定的7-降冰片阳离子是Story等人在1960年通过在-80℃下将降冰片与四氟硼酸银在二氧化硫中反应制备的。核磁共振谱显示,它是非经典桥接的(第一个观察到的稳定的非经典离子)。
1962年,Olah通过核磁共振直接观察到,在将叔丁基氟化物溶解在魔酸中时,叔丁基碳化物是一个稳定物种。Schleyer等人首次报告了降冰片阳离子的核磁共振,Saunders等人证明它在一个屏障上进行了质子扰动。
属性
在有机化学中,碳化物常常是被亲核剂(如羟基(OH−)离子或卤素离子)攻击的目标。
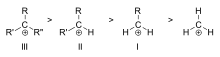
根据与电离碳结合的碳原子数量,碳化物可分为一级、二级或三级。初级碳化物有一个或零个碳原子连接到电离碳上,二级碳化物有两个碳原子连接到电离碳上,三级碳化物有三个碳原子连接到电离碳上。
碳化物的稳定性随着与带电荷的碳结合的烷基数量而增加。三级碳化物比二级碳化物更稳定(并且更容易形成);一级碳化物非常不稳定,因为虽然电离的高阶碳化物通过超共轭而稳定,但未被取代的(一级)碳化物却不稳定。因此,如果会形成一个初级碳化物,通常不会发生NS1反应和E1消除反应等反应。当电离碳旁边有一个碳-碳双键时,则是一个例外。像烯丙基阳离子CH2=2+CH-CH和苄基阳离子CH65-2+CH这样的阳离子比大多数其他碳化物更稳定。能够形成烯丙基或苄基碳化物的分子特别具有反应性。
碳化物从较不稳定的结构向同样稳定或更稳定的结构发生重排反应,其速率常数超过109/秒。这一事实使许多化合物的合成途径变得复杂。例如,当3-戊醇与盐酸水溶液一起加热时,最初形成的3-戊基碳化物会重新排列成3-戊基和2-戊基的统计混合物。这些阳离子与氯离子反应,产生大约1/3的3-氯戊烷和2/3的2-氯戊烷。
一些碳化物,如降冰片阳离子,表现出或多或少的对称三中心结合。这类阳离子被称为非经典离子。经典 "碳化物和 "非经典 "异构体之间的能量差异通常非常小,而且在 "经典 "和 "非经典 "结构之间的转换通常很少,甚至没有任何活化能。2-丁基碳化物的 "非经典 "形式本质上是2-丁烯,其质子直接位于碳-碳双键的中心上方。"非经典 "的碳配位曾经是巨大争议的主题。乔治-奥拉对化学的最大贡献之一就是解决了这个争议。
特定的碳化物
可以通过核磁共振来研究环丙基卡宾基阳离子。
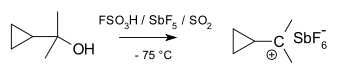
在一个二甲基衍生物的核磁共振谱中,发现两个甲基有两个不相等的信号,表明这个阳离子的分子构象不是垂直的(如A),而是二分的(如B),空的p轨道和环丙基环系统在同一个平面上。
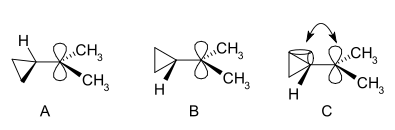
在弯曲键理论方面,这种偏好可以通过假设填充的环丙烷弯曲键和空的p轨道之间有有利的轨道重叠来解释。
问题和答案
问:什么是碳化物?
答:碳化物是一种带有正电荷的碳原子的离子。
问:什么是碳配位体的外价壳?
答:碳配位体的外层价层只有六个电子,而不是稳定的八个价层电子。
问:为什么碳化物常常具有反应性?
答:碳化物常常是反应性的,因为它们试图填补八价电子,并重新获得中性电荷。
问:碳原子的最大稳定性是什么?
答:当碳原子有八个价电子时,其稳定性达到最大。
问:什么是化学中的六重奏?
答:六价电子是一个术语,用于描述碳原子在碳化物中的外价壳中只有六个电子,而不是稳定的八个价电子。
问:什么是碳配位体的杂化和分子几何?
答:虽然从逻辑上讲,碳配位体具有sp3杂化,空的sp3轨道带有正电荷,但其反应性更接近于sp2杂化,具有三叉平面的分子几何结构。
问:什么是八边形规则?
答:八边形规则是化学中的一个原则,它指出原子倾向于与其他原子形成化学键,使两个原子都有一组稳定的八个价电子。