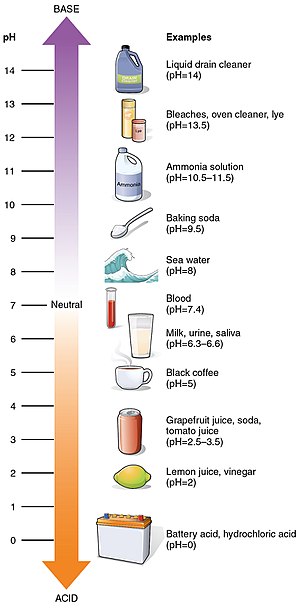
pH值是一个从0到14的酸度表。它显示物质的酸性或碱性。酸性越高的溶液,pH值越低。碱性越强的溶液pH值越高。不是酸性或碱性的物质(即中性溶液)的pH值通常为7,酸性物质的pH值小于7。碱性物质的pH值大于7。
pH值是衡量溶液中质子(H+)浓度的指标。S.P.L.Sørensen在1909年提出这个概念。p代表德语potenz,意思是功率或浓度,H代表氢离子(H+)。
计算pH值最常用的公式是:。
pH值 = - log 10 [H +] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}}。
[H+]表示H+离子的浓度(也写成[H3O+],即等浓度的氢离子),单位是摩尔/升(也称摩尔度)。
然而,正确的公式其实是。
pH值 = - log 10 [a H +] {\displaystyle {\mbox{pH}}=-\log _{10}/left[a_{\mathrm {H^{+}}}}/right]}。
其中a H + {\displaystyle a_{\mathrm {H^{+}}。
大多数物质的pH值在0-14之间,尽管极度酸性或碱性物质的pH值可能<0,或pH值>14。
碱性物质的氢离子浓度不是氢离子,而是氢氧离子(OH-)。
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)