SN 2反应(也被称为双分子亲核取代)是有机化学中的一个取代反应。它是亲核取代的一种类型,亲核者的孤对攻击一个电子不足的亲电中心并与之结合。这就排出了另一个叫做 "离去基团 "的基团。因此,进入的基团在一个步骤中取代了离开的基团。由于两个反应物参与了反应的缓慢、决定速度的步骤,这导致了双分子亲核取代的名称,或SN 2。在无机化学家中,SN 2反应通常被称为互换机制。
SN2反应
反应机制
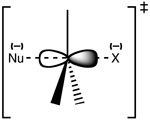
该反应通常发生在一个脂肪族的sp3 碳中心,该碳中心上有一个电负性的、稳定的离去基团--'X'--经常是一个卤化物原子。C-X键的断裂和新的C-Nu键的形成同时发生,形成一种过渡状态,在这种状态下,受到亲核攻击的碳是五重的,并且大约是sp2 杂化。亲核者攻击与离去基团成180°的碳,因为这提供了亲核者的孤对和C-X σ*反键轨道之间的最佳重叠。然后离开的基团被推到对面,形成了产品。
如果亲核攻击下的底物是手性的,这可能会导致(尽管不一定)立体化学的反转,称为Walden反转。
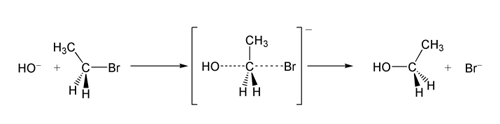
在SN 2反应的一个例子中,OH −(亲核派)对溴乙烷(亲电派)的攻击导致了乙醇的产生,溴化物作为离开基团被喷出。
如果背面的攻击路线没有被分子中的其他原子阻挡(被底物上的取代物立体阻碍),就会发生SN 2反应。所以,这种机制通常发生在一个无阻碍的主碳中心。如果离去基团附近的底物上有立体拥挤,例如在一个三级碳中心,取代将使用SN 1而不是SN 2机制,(SN 1也更有可能发生在受阻的分子上,因为可以形成足够稳定的碳化物中介)。
在配位化学中,关联取代的机制与SN 2相似。
影响反应速度的因素
有四个因素影响反应的速度。
- 底物。底物在决定反应的速度方面起着最重要的作用。这是因为亲核体从底物的背面发起攻击,从而破坏离碳基团键并形成碳-亲核体键。因此,为了最大限度地提高SN 2反应的速率,底物的背面必须尽可能不受阻碍。总的来说,这意味着甲基和一级底物的反应最快,其次是二级底物。三级底物不参与SN 2反应,因为有立体阻碍。
- 亲核派。与底物一样,立体阻碍影响亲核体的强度。例如,甲氧基阴离子既是强碱又是亲核体,因为它是一个甲基亲核体,因此非常不受阻碍。另一方面,叔丁氧是强碱,但亲核性差,因为它的三个甲基阻碍了它对碳的接近。亲核力量也受电荷和电负性的影响:亲核性随着负电荷的增加和电负性的降低而增加。例如,OH- 是比水更好的亲核体,而I- 是比Br- 更好的亲核体(在极性的亲溶剂中)。在极性非protic溶剂中,由于溶剂和亲核体之间没有氢键,亲核性在元素周期表中会向上增加一列。在这种情况下,亲核性反映了碱性。因此,I- 将是一个比Br- 更弱的亲核体,因为它是一个弱碱。
- 溶剂。溶剂会影响反应速度,因为溶剂可能会也可能不会包围亲核派,从而阻碍或不阻碍其接近碳原子。极性非专业溶剂,如四氢呋喃,是比极性亲属溶剂更适合这种反应的溶剂,因为极性亲属溶剂将被溶剂与亲核体的氢键所溶解。这阻碍了它对带有离去基团的碳的攻击。
- 离去基团。离去基团会影响反应的速度。离去基团越稳定,当亲核派攻击碳时,它就越有可能将其离碳基团的两个电子与之结合。因此,作为共轭碱的离开基团越弱,离开基团越好。同样地,其对应的酸越强,离去基团越好。好的离去基团的例子是卤化物(氟化物除外)和甲苯磺酸盐。但HO- 和 H2 N- 不是好的离去基团。
反应动力学
SN 2反应的速率是二阶的,因为决定速率的步骤取决于亲核体的浓度,[Nu− ]以及底物的浓度,[RX]。
r = k[RX][Nu− ]
这是SN 1和SN 2机制之间的一个关键区别。在SN 1反应中,亲核派在限速步骤结束后才攻击。但在SN 2反应中,亲核者在限制步骤中强迫离开基团。换句话说,SN 1反应的速率只取决于底物的浓度,而SN 2反应的速率则取决于底物和亲核物的浓度。在两种机制都有可能的情况下(例如在二级碳中心),机制取决于溶剂、温度、亲核物的浓度或离去基团。
SN 2反应通常在一级烷基卤化物或二级烷基卤化物与无机溶剂中进行。由于立体阻碍,它们在三级烷基卤化物中的发生率可以忽略不计。
SN 2和SN 1是反应的滑动尺度的两个极端。有可能发现许多反应在其机制中同时表现出SN 2和SN 1的特征。例如,有可能得到一个由烷基卤化物形成的接触离子对,其中的离子没有完全分开。当这些离子发生置换时,许多反应分子的立体化学将被颠倒(如SN 2),但也有少数分子可能显示配置的保留。SN 2反应比SN 1反应更常见。
E2竞争
绕行机制
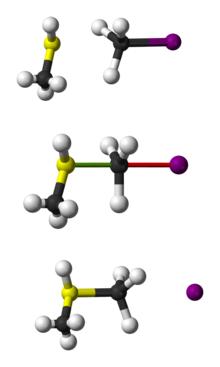
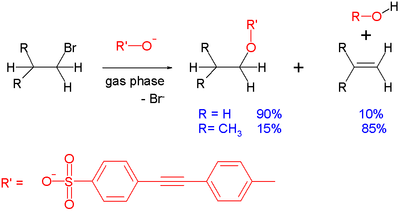
2008年引起关注的一项发展涉及到在氯离子和甲基碘之间的气相反应中用一种叫做交叉分子束成像的特殊技术观察到的SN 2迂回机制。当氯离子有足够的速度时,碰撞后产生的碘化物离子的能量比预期的要低得多,据推测,在实际位移发生之前,由于甲基在碘原子周围的完全绕行而损失了能量。
相关页面
- 取代反应
- SN 1反应
问题和答案
问:什么是SN2反应?
答:SN2反应是有机化学中的一种取代反应,亲核体攻击缺电子的亲电中心,排出一个离去基团,然后一步步取代它。
问:SN2反应是一种什么样的取代反应?
答:SN2反应是亲核取代反应的一种。
问:在SN2反应的慢速、决定速度的步骤中,有多少种反应物参与?
答:有两个反应物参与SN2反应的慢速、决定速度的步骤。
问:SN2反应的名称 "双分子亲核取代 "的含义是什么?
答:SN2反应的名称 "双分子亲核取代 "是指两个反应物参与反应的慢速决定步骤。
问:在SN2反应的背景下,什么是亲核物?
答:亲核体是指捐出一对孤电子以形成化学键的分子或离子。
问:在SN2反应的背景下,什么是亲电子?
答:亲电子是指接受一对电子以形成化学键的分子或离子。
问:在无机化学家中,SN2反应通常被称为什么?
答:在无机化学家中,SN2反应常被称为互换机制。